Exubera diabeedi raviks
Brändinimi: Exubera
Üldnimi: humaaninsuliin
Annustamisvorm: inhalatsioonipulber
Sisu:
Kirjeldus
Kliiniline farmakoloogia
Kliinilised uuringud
Näidustused ja kasutamine
Vastunäidustused
Hoiatused
Ettevaatusabinõud
Ravimite koostoimed
Kõrvaltoimed
Üleannustamine
Annustamine ja manustamine
Kuidas komplektis
Exubera, inimese insuliin [rDNA päritolu] Patsiendi teave (lihtsas inglise keeles)
Kirjeldus
Exubera® koosneb humaaninsuliini inhalatsioonipulbrit sisaldavatest villidest, mida manustatakse Exubera abil® Sissehingaja. Exubera villid sisaldavad humaaninsuliini, mis on toodetud rekombinantse DNA tehnoloogia abil, kasutades mittepatogeenset Escherichia coli (K12) laboratoorset tüve. Keemiliselt on humaaninsuliinil empiiriline valem C257H383N65O77S6 ja molekulmass 5808. Humaaninsuliinil on järgmine primaarne aminohapete järjestus:
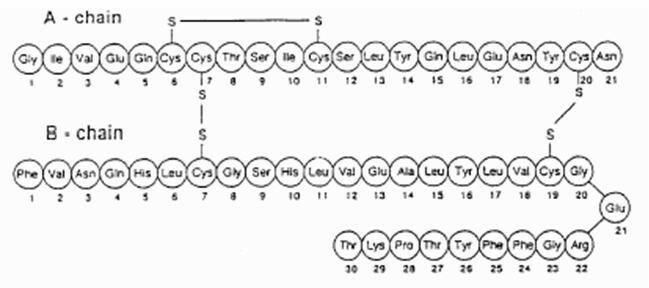
Exubera (inimese insuliin [rDNA päritolu). Inhalatsioonipulber on valge kuni valkjas pulber ühikannusega blistris (täitmismass, vt tabel 1). Iga Exubera ühikannusega blister sisaldab 1 mg või 3 mg insuliini annust (vt tabel 1) homogeenne pulbriline preparaat, mis sisaldab naatriumtsitraati (dihüdraati), mannitooli, glütsiini ja naatriumi hüdroksiid. Pärast Exubera blistri sisestamist inhalaatorisse pumpab patsient inhalaatori käepideme ja vajutab nuppu, mis põhjustab blistri läbistamist. Seejärel dispergeeritakse insuliini inhalatsioonipulber kambrisse, lastes patsiendil sisse hingata aerosoolpulbri.
Standardiseeritud in vitro katsetingimustes väljastab Exubera inhalaatori huulikust spetsiifilise emiteeritud annuse insuliini (vt tabel 1). Osa osakeste kogumassist eraldub peente osakestena, mis suudavad jõuda sügavasse kopsu. Blistris võib olla kuni 45% 1 mg blistri sisust ja kuni 25% 3 mg blistri sisust.
Tabel 1: Annuste nomenklatuur ja teave
| Täida missa (mg pulbrit) |
Nominaalne annus (mg insuliini) |
Emissiooniannus*,†(mg insuliini) |
Peenosakeste annusc,†(mg insuliini) |
|---|---|---|---|
| |||
| 1.7 | 1.0 | 0.53 | 0.4 |
| 5.1 | 3.0 | 2.03 | 1.0 |
Kopsu tarnitud tegelik insuliini kogus sõltub patsiendi individuaalsetest teguritest, näiteks sissehingamise voolu profiil. In vitro ei mõjuta aerosoolide eraldumine mõõdetavaid voolukiirusi üle 10 L / min.
ülaosa
Kliiniline farmakoloogia
Toimemehhanism
Insuliini peamine tegevus on glükoosi metabolismi reguleerimine. Insuliin alandab vere glükoosikontsentratsiooni, stimuleerides perifeerset glükoosivarustust skeletilihastes ja rasvas ning pärssides maksa glükoositootmist. Insuliin pärsib lipolüüsi adipotsüüdis, pärsib proteolüüsi ja soodustab valkude sünteesi.
Farmakokineetika
Imendumine
Exubera väljastab insuliini suu kaudu sissehingamise teel. Insuliin imendub sama kiiresti kui subkutaanselt manustatud kiiretoimelised insuliini analoogid ja kiiremini kui subkutaanselt manustatav regulaarne humaaninsuliin tervetel isikutel ja I või II tüüpi diabeediga patsientidel (vt Joonis 1).
Joonis 1: Pärast 2. tüüpi diabeedi patsientide vaba insuliini seerumi kontsentratsiooni keskmisi muutusi (µU / ml) Exuberast (6 mg) sissehingatava insuliini ja subkutaanse regulaarse iniminsuliini üksikannuste manustamine (18U)
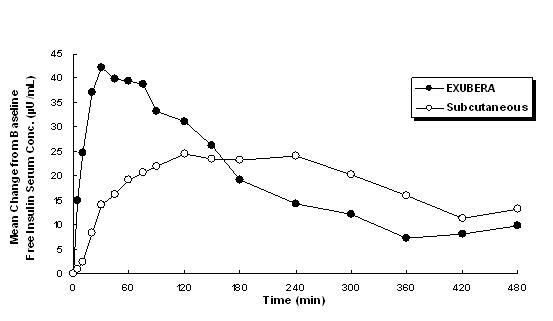
1. ja 2. tüüpi diabeediga patsientide kliinilistes uuringutes saavutas seerumi insuliini maksimaalne kontsentratsioon pärast Exubera sissehingamist kiiremini kui pärast tavalise iniminsuliini subkutaanset süstimist 49 minutit (vahemik 30 kuni 90 minutit) võrreldes 105 minutiga (vahemik 60 kuni 240 minutit), vastavalt.
Kliinilistes uuringutes vähenes regulaarse subkutaanse humaaninsuliini imendumine patsiendi kehamassiindeksi (KMI) suurenemisega. Pärast Exubera sissehingamist ei olnud insuliini imendumine aga KMI-st sõltumatu.
Tervetel inimestel läbiviidud uuringus süstemaatiline insuliini ekspositsioon (AUC ja Cmax) pärast Exubera suurenes annusega vahemikus 1-6 mg, kui seda manustati kombinatsioonis 1 ja 3 mg villid.
Uuringus, kus võrreldi kolme 1 mg blistri annustamisvormi ühe 3 mg blistriga, Cmax ja AUC pärast kolm 1 mg blistrit olid vastavalt umbes 30% ja 40% suuremad kui pärast ühe 3 mg blistri manustamist (vt ANNUSTAMINE JA HALDAMINE).
Levitamine ja kõrvaldamine
Kuna rekombinantne humaaninsuliin on identne endogeense insuliiniga, on süsteemne jaotumine ja eliminatsioon eeldatavalt sama. Exubera puhul pole see aga kinnitust leidnud.
Farmakodünaamika
Nagu ka subkutaanselt manustatavad kiiretoimelised insuliini analoogid, on Exuberal glükoosisisaldust langetav toime kiirem kui subkutaanselt manustataval tavalisel humaaninsuliinil. Tervetel vabatahtlikel oli Exubera glükoosisisaldust vähendav toime võrreldav subkutaanselt manustatud regulaarne humaaninsuliin ja pikem kui subkutaanselt manustatavad kiiretoimelised insuliinianaloogid (vt Joonis 2).
Joonis 2. Keskmine glükoosi infusioonikiirus (GIR) normaliseeritud GIR-nimax iga patsiendi ravi versus aeg tervetel vabatahtlikel
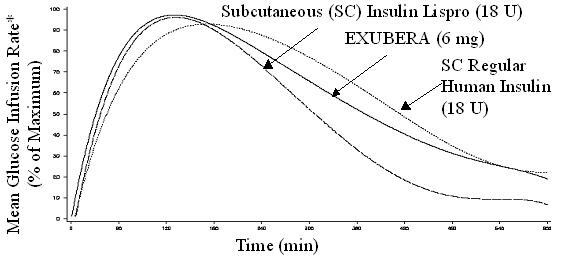
* Määratud glükoosikogusena, mis on infundeeritud püsiva plasma glükoosikontsentratsiooni säilitamiseks, normaliseeritud maksimaalsetele väärtustele (protsent maksimaalsetest väärtustest); mis näitab insuliini aktiivsust.
Exubera sissehingamisel ilmneb tervetel vabatahtlikel glükoosisisaldust vähendav toime 10-20 minuti jooksul. Maksimaalne toime glükoosisisalduse vähenemisele avaldub umbes 2 tundi pärast sissehingamist. Glükoosisisaldust vähendav toime kestab umbes 6 tundi.
1. või 2. tüüpi diabeediga patsientidel on Exuberal suurem glükoosisisaldust langetav toime esimese kahe tunni jooksul pärast annustamist, võrreldes subkutaanselt manustatud tavalise humaaninsuliiniga.
Exubera glükoosisisaldust langetava aktiivsuse subjektsisene varieeruvus on üldiselt võrreldav subkutaanselt manustatava regulaarse humaaninsuliiniga 1. ja 2. tüüpi diabeediga patsientidel.
Eripopulatsioonid
Pediaatrilised patsiendid
I tüüpi diabeediga lastel (6–11 aastat) ja noorukitel (12–17 aastat) oli Exubera insuliini maksimaalse kontsentratsiooni saavutamise aeg saavutatakse kiiremini kui subkutaanse regulaarse humaaninsuliini puhul, mis on kooskõlas 1. tüüpi täiskasvanud patsientide vaatlustega diabeet.
Geriaatrilised patsiendid
Exubera farmakokineetilistes omadustes pole ilmseid erinevusi, kui võrrelda üle 65-aastaseid ja nooremaid täiskasvanud patsiente.
Sugu
Diabeediga ja ilma diabeedita isikutel ei täheldatud Exubera farmakokineetilistes omadustes ilmseid erinevusi meeste ja naiste vahel.
Rass
Uuring viidi läbi 25 terve Kaukaasia ja Jaapani mittediabeediga katsealusega Exubera farmakokineetilised ja farmakodünaamilised omadused võrreldes tavalise inimese nahaaluse süstimisega insuliin. Exubera farmakokineetilised ja farmakodünaamilised omadused olid kahe populatsiooni vahel võrreldavad.
Rasvumine
Exubera imendumine ei sõltu patsiendi KMI-st.
Neerukahjustus
Neerukahjustuse mõju Exubera farmakokineetikale ei ole uuritud. Neerufunktsiooni häiretega patsientidel võib osutuda vajalikuks hoolikas glükoosisisalduse jälgimine ja insuliini annuse kohandamine (vt ETTEVAATUSABINÕUD, Neerukahjustus).
Maksakahjustus
Maksakahjustuse mõju Exubera farmakokineetikale ei ole uuritud. Maksapuudulikkusega patsientidel võib olla vajalik hoolikas glükoosisisalduse jälgimine ja insuliini annuse korrigeerimine (vt ETTEVAATUSABINÕUD).
Rasedus
Exubera imendumine rasedatel ja raseduseelse II tüüpi suhkurtõvega patsientidel oli sama kui II tüüpi diabeediga rasedatel (vt lõik 2). ETTEVAATUSABINÕUD).
Suitsetamine
Suitsetajatel on Exubera süsteemne insuliini ekspositsioon eeldatavalt 2–5 korda kõrgem kui mittesuitsetajatel. Exubera on vastunäidustatud patsientidele, kes suitsetavad või on loobunud suitsetamisest vähem kui 6 kuud enne Exubera-ravi alustamist. Kui patsient hakkab suitsetama või jätkab suitsetamist, tuleb Exubera hüpoglükeemia suurenenud riski tõttu viivitamatult katkestada ja kasutada alternatiivset ravi (vt VASTUNÄIDUSTUSED).
Exubera kliinilistes uuringutes, milles osales 123 patsienti (neist 69 olid suitsetajad), esines suitsetajatel glükoosisisaldust langetava toime kiirem ilmnemine. suurem maksimaalne toime ja suurem glükoosisisaldust langetav toime (eriti esimese 2-3 tunni jooksul pärast annustamist), võrreldes mittesuitsetajad.
Passiivne sigaretisuits
Vastupidiselt aktiivse suitsetamise järgselt suurenenud insuliini ekspositsioonile, kui Exuberat manustati 30 tervele suitsetamata vabatahtlikule pärast 2 tundides kokkupuudet passiivse sigaretisuitsuga kontrollitud eksperimentaalses keskkonnas, vähenesid insuliini AUC ja Cmax umbes 20% ja 30%, vastavalt. Exubera farmakokineetikat ei ole uuritud suitsetajatel, kes puutuvad krooniliselt kokku passiivse sigaretisuitsuga.
Aluseliste kopsuhaigustega patsiendid
Exubera kasutamist patsientidel, kellel on põhihaigused, näiteks astma või KOK, ei soovitata, kuna Exubera ohutus ja efektiivsus selles populatsioonis pole tõestatud (vt HOIATUSED). Exubera kasutamine on vastunäidustatud patsientidele, kellel on ebastabiilne või halvasti juhitav kopsuhaigus, kuna see on lai kopsufunktsiooni muutused, mis võivad mõjutada Exubera imendumist ja suurendada hüpoglükeemia või hüperglükeemia (vt VASTUNÄIDUSTUSED).
Farmakokineetilises uuringus 24 kerge diabeediga diabeediga isikul, pärast insuliini imendumist Exubera oli bronhodilataatoriga ravi puudumisel umbes 20% madalam kui imendunud patsientidel, kellel seda ei olnud astma. Kuid uuringus, mis hõlmas 24 mittediabeetikut, kellel oli krooniline obstruktiivne kopsuhaigus (KOK), kokkupuude pärast Exubera manustamist oli umbes kaks korda suurem kui normaalsetel isikutel, kellel seda ei olnud KOK (vt ETTEVAATUSABINÕUD).
Albuterooli manustamine 30 minutit enne Exubera manustamist mittediabeetikutele, kellel on nii kerge astma (n = 36) kui ka mõõdukas astma (n = 31) tagajärjel suurenes insuliini AUC ja Cmax keskmiselt 25–50% võrreldes Exubera üksi manustamisega (vt ETTEVAATUSABINÕUD).
ülaosa
Kliinilised uuringud
Exubera ohutust ja efektiivsust on uuritud umbes 2500 täiskasvanud I ja II tüüpi diabeediga patsiendil. Enamiku uuringute esmane efektiivsuse parameeter oli glükeemiline kontroll, mida mõõdeti hemoglobiini A1c (HbA1c) vähenemisega võrreldes algtasemega.
1. tüüpi diabeet
I tüüpi diabeediga patsientidega viidi läbi 24-nädalane randomiseeritud avatud aktiivse kontrolli uuring (uuring A), et hinnata ravi ohutust ja efektiivsust. Exubera manustati enne sööki kolm korda päevas (TID) koos Humulin® U Ultralente® (humaaninsuliini pikendatud tsingi suspensioon) öösel ühe süstiga (n = 136). Võrdlusravi oli nahaalune regulaarne humaaninsuliin, mida manustati kaks korda päevas (BID) (hommikueine ja õhtusöök) NPH humaaninsuliini (humaaninsuliini isofaani suspensioon) kaks korda päevas süstimisega (n = 132). Selles uuringus oli keskmine vanus 38,2 aastat (vahemik: 20–64) ja 52% katsealustest olid mehed.
I tüüpi diabeediga patsientidel viidi läbi teine 24-nädalane randomiseeritud avatud aktiivse kontrolli uuring (uuring B), et hinnata Exubera (n = 103) ohutus ja efektiivsus võrreldes subkutaanse regulaarse humaaninsuliiniga (n = 103), kui seda manustati kolm korda enne manustamist söögikorrad. Mõlemas ravirühmas manustati NPH humaaninsuliini kaks korda kaks korda (hommikul ja enne magamaminekut) põhinsuliinina. Selles uuringus oli keskmine vanus 38,4 aastat (vahemik: 19–65) ja 54% katsealustest olid mehed.
Igas uuringus olid HbA1c vähenemine ja hüpoglükeemia määr kahes ravirühmas võrreldavad. Exubera'ga ravitud patsientidel vähenes tühja kõhuga plasma glükoosisisaldus rohkem kui võrdlusrühmas. Patsientide protsent, kes saavutasid HbA1c taseme <8% (Ameerika Diabeedi Assotsiatsiooni ravimeetme kohta) Tase uuringu läbiviimise ajal) ja HbA1c tase <7% oli kahe ravirühma vahel võrreldav. Uuringute A ja B tulemused on toodud tabelis 2.
Tabel 2: Kahe 24-nädalase aktiivse kontrolli ja avatud märgisega uuringu tulemused 1. tüüpi diabeediga patsientidel (uuringud A ja B)
| Uuring A | Uuring B | |||
|---|---|---|---|---|
| Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) | Exubera (TID) + NPH (BID) | SC R (TID) + NPH (BID) | |
| Näidissuurus | 136 | 132 | 103 | 103 |
| UL = Humuliin® U ülimalt hea®; SC R = subkutaanne regulaarne humaaninsuliin | ||||
| ||||
| HbA1c (%) | ||||
| Algjoone keskmine | 7.9 | 8.0 | 7.8 | 7.8 |
| Adj. keskmine muutus algtasemest | -0.2 | -0.4 | -0.3 | -0.2 |
| Exubera miinus SC R* | 0.14 | -0.11 | ||
| Ravi erinevuse korral 95% CI | (-0.03, 0.32) | (-0.30, 0.08) | ||
| Tühja kõhuga plasma glükoos (mg / dL) | ||||
| Algjoone keskmine | 191 | 198 | 178 | 191 |
| Adj. keskmine muutus algtasemest | -32 | -6 | -23 | 13 |
| Exubera miinus SC R | -27 | -35 | ||
| Ravi erinevuse korral 95% CI | (-47, -6) | (-58, -13) | ||
| 2-tunnine postrandiaalne glükoosikontsentratsioon (mg / dL) | ||||
| Algjoone keskmine | 283 | 305 | 273 | 293 |
| Adj. keskmine muutus algtasemest | -21 | 14 | -1 | -3 |
| Exubera miinus SC R | -35 | 2 | ||
| Ravi erinevuse korral 95% CI | (-61, -8) | (-29, 32) | ||
| Patsiendid, kellel on uuringu lõpus HbA1c < 8%†| 64.0% | 68.2% | 74.8% | 66.0% |
| Patsiendid, kellel on uuringu lõpus HbA1c < 7% | 16.9% | 19.7% | 28.2% | 30.1% |
| Kehakaal | ||||
| Algväärtuse keskmine (kg) | 77.4 | 76.4 | 76.0 | 76.9 |
| Adj. keskmine muutus algtasemest (kg) | 0.4 | 1.1 | 0.4 | 0.6 |
| Exubera miinus SC R | -0.72 | -0.24 | ||
| Ravi erinevuse korral 95% CI | (-1.48, 0.04) | (-1.07, 0.59) | ||
| Uuringu lõpuks päevane insuliiniannus | ||||
| Lühitoimeline insuliin | 13,4 mgc | 18,3 RÜ | 10,9 mgc | 25,7 RÜ |
| Pikatoimeline insuliin | 26,4 RÜ | 37,1 RÜ | 31,5 RÜ | 31,9 RÜ |
2. tüüpi diabeet
Monoteraapia patsientidel, kelle toitumine ja treeningravi ei ole optimaalselt kontrollitud
12-nädalane randomiseeritud avatud aktiivse kontrolli uuring (uuring C) viidi II tüüpi diabeediga patsientidel läbi mitte optimaalselt kontrollides dieedi ja treeninguga, hinnatakse söögieelse TID Exubera (n = 75) ohutust ja efektiivsust võrreldes insuliini sensibiliseeriv aine. Selles uuringus oli keskmine vanus 53,7 aastat (vahemik: 28–80), 55% katsealustest olid mehed ja keskmine kehamassiindeks 32,3 kg / m2.
12 nädala pärast HbA1c Exuberaga ravitud patsientide tase langes 2,2% (SD = 1,0), võrreldes algtasemega 9,5% (SD = 1,1). Exuberaga ravitud patsientide osakaal, kes saavutas uuringu lõpus HbA1c tase <8% tõusis 82,7% -ni. Exuberaga ravitud patsientide osakaal, kes saavutas uuringu lõpus HbA1c tase
Monoteraapia ja lisateraapia patsientidel, keda on varem ravitud suu kaudu manustatava ravimiga
Tüübiga patsientidega viidi läbi 12-nädalane randomiseeritud avatud aktiivse kontrolli uuring (uuring D) 2 diabeeti, kes said praegu ravi, kuid olid halvasti kontrolli all, kahe suukaudse ravimiga (OA). Algväärtuse OA-d hõlmasid insuliini sekretsiooni andjat ja kas metformiini või tiasolidiindiooni. Patsiendid randomiseeriti ühte kolmest rühmast: ainult OA-ravi jätkamine (n = 96), üleminek ravile söögieelne TID Exubera monoteraapia (n = 102) või söögieelse TID Exubera lisamine jätkuvale OA-ravile (n = 100). Selles uuringus oli keskmine vanus 57,4 aastat (vahemik: 33–80), 66% katsealustest olid mehed ja keskmine kehamassiindeks oli 30 kg / m2.
Exubera monoteraapia ja Exubera kombinatsioonis OA-raviga olid HbA vähendamisel paremad kui ainult OA-ravi1c tasemed algtasemest. Hüpoglükeemia esinemissagedus kahes Exubera ravirühmas oli pisut kõrgem kui ainult OA-ravi rühmas. Ainult OA-raviga võrreldes on HbA-tasemega patsientide protsent1c tase <8% (Ameerika Diabeediliidu ravitoime taseme kohta uuringu tegemise ajal) ja HbA1c tase <7% oli kõrgem patsientidel, keda raviti Exubera monoteraapia ja Exubera kombinatsioonis OA-raviga. Mõlema Exubera ravirühma patsientidel esines tühja kõhuga plasma glükoosisisalduse langus rohkem kui patsientidel, kes said ainult OA-ravi. Uuringu D tulemused on toodud tabelis 3.
Tabel 3: 12-nädalase aktiivse kontrolli ja avatud märgisega uuringu tulemused II tüüpi diabeediga patsientidel, kelle suukaudsete suukaudsete ravimite teraapia ei ole optimaalselt kontrolli all (uuring D)
| Uuring D | Exubera monoteraapia | OAs* | Exubera + OA-d |
|---|---|---|---|
| Näidissuurus | 102 | 96 | 100 |
| |||
| HbA1c (%) | |||
| Algjoone keskmine | 9.3 | 9.3 | 9.2 |
| Adj. keskmine muutus algtasemest | -1.4 | -0.2 | -1.9 |
| Exubera rühm miinus OA-d†| -1.18†,c, § | -1.67†, ¶, § | |
| Ravi erinevuse korral 95% CI | (-1.41, -0.95) | (-1.90, -1.44) | |
| Tühja kõhuga plasma glükoos (mg / dL) | |||
| Algjoone keskmine | 203 | 203 | 195 |
| Adj. keskmine muutus algtasemest | -23 | 1 | -53 |
| Exubera rühm miinus OA-d | -24c | -53 ¶ | |
| Ravi erinevuse korral 95% CI | (-36, -11) | (-66, -41) | |
| Patsiendid, kellel on uuringu lõpus HbA1c < 8%# | 55.9% | 18.8% | 86.0% |
| Patsiendid, kellel on uuringu lõpus HbA1c < 7% | 16.7% | 1.0% | 32.0% |
| Kehakaal | |||
| Algväärtuse keskmine (kg) | 89.5 | 88.0 | 88.6 |
| Adj. keskmine muutus algtasemest (kg) | 2.8 | 0.0 | 2.7 |
| Exubera rühm miinus OA-d | 2.80c | 2.75 ¶ | |
| Ravi erinevuse korral 95% CI | (1.94, 3.65) | (1.89, 3.61) |
24-nädalane randomiseeritud avatud aktiivse kontrolli uuring (uuring E) viidi läbi 2. tüüpi diabeediga patsientidel, kes saavad praegu sulfonüüluurearavi. Selle uuringu eesmärk oli hinnata söögieelse Exubera manustamise jätkamise ohutust ja tõhusust sulfonüüluurearavi (n = 214) võrreldes söögieelse metformiini lisamisega jätkuvale sulfonüüluurearavile (n = 196). Isikud kihistati vastavalt HbA1c-le 1. nädalal. Määratleti kaks kihti: madal HbA1c kiht (HbA1c â ‰% 8% –9,5%) ja kõrge HbA1c kiht (HbA1c > 9,5 kuni –12%).
Exubera kombinatsioonis sulfonüüluureaga oli HbA1c väärtuste vähendamisel algtasemest kõrgema kihi rühmas parem kui metformiin ja sulfonüüluurea. Exubera kombinatsioonis sulfonüüluureaga oli HbA1c väärtuste vähendamisel madala kihistusega rühmas võrreldav metformiiniga kombinatsioonis sulfonüüluureaga. Hüpoglükeemia määr oli kõrgem pärast Exubera lisamist sulfonüüluurea kui pärast metformiini lisamist sulfonüüluurea. HbA1c sihtväärtuseni 8% ja 7% jõudnud patsientide protsent oli mõlemas kihis ravirühmade vahel võrreldav, nagu ka tühja kõhu plasma glükoosisisalduse vähenemine (vt Tabel 4).
Teine 24-nädalane randomiseeritud avatud aktiivse kontrolli uuring (uuring F) viidi läbi II tüüpi diabeediga patsientidel, kes saavad praegu metformiinravi. Selle uuringu eesmärk oli hinnata söögieelse Exubera manustamise jätkamise ohutust ja tõhusust metformiinravi (n = 234), võrreldes söögieelse glibenklamiidi lisamisega jätkuvale metformiinravile (n = 222). Selle uuringu subjektid kihistuti ka ühte kahest kihist, nagu on määratletud uuringus E.
Exubera kombinatsioonis metformiiniga oli HbA vähendamisel parem kui glibenklamiid ja metformiin1c väärtused algtasemest ja eesmärgi HbA saavutamine1c kõrge kihirühma väärtused. Exubera kombinatsioonis metformiiniga oli HbA vähendamisel võrreldav glibenklamiidiga kombinatsioonis metformiiniga1c väärtused algtasemest ja eesmärgi HbA saavutamine1c väärtused madala kihi rühmas. Hüpoglükeemia määr oli pärast Exubera lisamist metformiinile veidi kõrgem kui pärast glibenklamiidi lisamist metformiinile. Tühja kõhuga plasma glükoosisisalduse langus oli ravirühmade vahel võrreldav (vt Tabel 4).
Tabel 4: Kahe 24-nädalase aktiivse kontrolli ja avatud märgisega uuringu tulemused varem II tüüpi diabeediga patsientidel, kes on varem saanud suu kaudu ravi (uuringud E ja F)
| Uuring E | Uuring F | |||||||
|---|---|---|---|---|---|---|---|---|
| Exubera + SU* | Kohtusime*+ SU* | Exubera + SU* | Kohtusime*+ SU* | Exubera + Met* | Gli* + Kohtunud* | Exubera + Met* | Gli* + Kohtunud* | |
| Kõrge kiht†| Madal kiht†| Kõrge kiht†| Madal kiht†| |||||
| Näidissuurus | 113 | 103 | 101 | 93 | 109 | 103 | 125 | 119 |
| ||||||||
| HbA1c (%) | ||||||||
| Algjoone keskmine | 10.5 | 10.6 | 8.8 | 8.8 | 10.4 | 10.6 | 8.6 | 8.7 |
| Adj. keskmine muutus algtasemest | -2.2 | -1.8 | -1.9 | -1.9 | -2.2 | -1.9 | -1.8 | -1.9 |
| Exubera miinus OAc | -0.38c, § | -0.07 | -0.37c, ¶ | 0.04 | ||||
| Ravi erinevuse korral 95% CI | (-0.63, -0.14) | (-0.33, 0.19) | (-0.62, -0.12) | (-0.19, 0.27) | ||||
| Tühja kõhuga plasma glükoos (mg / dL) | ||||||||
| Algjoone keskmine | 241 | 237 | 197 | 198 | 223 | 243 | 187 | 196 |
| Keskmine muutus algtasemest | -46 | -47 | -48 | -52 | -42 | -40 | -46 | -49 |
| Exubera miinus OA | 1 | 4 | -2 | 4 | ||||
| Ravi erinevuse korral 95% CI | (-11, 12) | (-8, 16) | (-14, 10) | (-7, 15) | ||||
| Uuringu lõpu HbA-ga subjektid1c < 8%# | 48.7% | 44.7% | 81.2% | 73.1% | 72.5% | 56.3% | 80.8% | 86.6% |
| Uuringu lõpu HbA-ga subjektid1c < 7% | 20.4% | 14.6% | 30.7% | 32.3% | 33.9% | 17.5% | 40.0% | 42.9% |
| Kehakaal | ||||||||
| Algväärtuse keskmine (kg) | 80.8 | 79.5 | 79.9 | 81.9 | 88.3 | 87.8 | 90.3 | 88.2 |
| Adj. keskmine muutus algtasemest (kg) | 3.6 | -0.0 | 2.4 | -0.3 | 2.8 | 2.5 | 2.0 | 1.6 |
| Exubera miinus OA | 3.60 | 2.67 | 0.26 | 0.38 | ||||
| Ravi erinevuse korral 95% CI | (2.81, 4.39) | (1.84, 3.51) | (-0.70, 1.21) | (-0.52, 1.27) |
Kasutamine patsientidel, keda on eelnevalt ravitud nahaaluse insuliiniga
2. tüüpi insuliiniga ravitud patsientidega viidi läbi 24-nädalane randomiseeritud avatud aktiivse kontrolli uuring (uuring G). suhkurtõbi, et hinnata Exubera manustatud söögieelse TID ohutust ja tõhusust ühekordse öise süstimisega Humuliin® U ülimalt hea® (n = 146), võrreldes subkutaanse regulaarse iniminsuliiniga, mida manustati kaks korda päevas (hommikueine ja õhtusöök) NPH humaaninsuliini kaks korda päevas süstimisega (n = 149). Selles uuringus oli keskmine vanus 57,5 aastat (vahemik: 23–80), 66% katsealustest olid mehed ja keskmine kehamassiindeks oli 30,3 kg / m2.
HbA langus algtasemest1c, protsent HbA-d saavutavatest patsientidest1c tase <8% (Ameerika Diabeediliidu ravitoime taseme kohta uuringu tegemise ajal) ja HbA1c tase <7%, samuti hüpoglükeemia määr olid ravirühmade vahel sarnased. Exubera'ga ravitud patsientidel vähenes tühja kõhuga plasma glükoosisisaldus rohkem kui võrdlusrühmas. Uuringu G tulemused on toodud tabelis 5.
Tabel 5. Varem subkutaanse insuliiniga ravitud II tüüpi diabeediga patsientide 24-nädalase aktiivse kontrolliga avatud uuringu tulemused (uuring G)
| Uuring G | Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) |
|---|---|---|
| Näidissuurus | 146 | 149 |
| UL = Humuliin® U ülimalt hea®; SC R = subkutaanne regulaarne humaaninsuliin | ||
| ||
| HbA1c (%) | ||
| Algjoone keskmine | 8.1 | 8.2 |
| Adj. keskmine muutus algtasemest | -0.7 | -0.6 |
| Exubera miinus SC R* | -0.07 | |
| Ravi erinevuse korral 95% CI | (-0.31, 0.17) | |
| Tühja kõhuga plasma glükoos (mg / dL) | ||
| Algjoone keskmine | 152 | 159 |
| Adj. keskmine muutus algtasemest | -22 | -6 |
| Exubera miinus SC R | -16.36 | |
| Ravi erinevuse korral 95% CI | (-27.09, -5.36) | |
| Patsiendid, kellel on uuringu lõpus HbA1c < 8%†| 76.0% | 69.1% |
| Patsiendid, kellel on uuringu lõpus HbA1c < 7% | 45.2% | 32.2% |
| Kehakaal | ||
| Algväärtuse keskmine (kg) | 90.6 | 89.0 |
| Adj. keskmine muutus algtasemest (kg) | 0.1 | 1.3 |
| Exubera miinus SC R | -1.28 | |
| Ravi erinevuse korral 95% CI | (-1.96, -0.60) | |
| Uuringu lõpuks päevane insuliiniannus | ||
| Lühitoimeline insuliin | 16,6 mgc | 25,5 RÜ |
| Pikatoimeline insuliin | 37,9 RÜ | 52,3 RÜ |
ülaosa
Näidustused ja kasutamine
Exubera on näidustatud diabeediga täiskasvanud patsientide raviks hüperglükeemia kontrolli all hoidmiseks. Exuberal on toime algus sarnane kiiretoimeliste insuliinianaloogidega ja selle glükoosisisaldust vähendav toime on võrreldav subkutaanselt manustatava regulaarse humaaninsuliiniga. I tüüpi diabeediga patsientidel tuleb Exuberat kasutada režiimides, mis sisaldavad pikema toimeajaga insuliini. II tüüpi diabeediga patsientidel võib Exuberat kasutada monoteraapiana või kombinatsioonis suukaudsete ravimite või pikema toimeajaga insuliinidega.
ülaosa
Vastunäidustused
Exubera on vastunäidustatud patsientidele, kes on ülitundlikud Exubera või selle abiainete suhtes.
Exubera on vastunäidustatud patsientidele, kes suitsetavad või on loobunud suitsetamisest vähem kui 6 kuud enne Exubera-ravi alustamist. Kui patsient hakkab suitsetama või jätkab suitsetamist, tuleb Exubera hüpoglükeemia suurenenud riski tõttu viivitamatult katkestada ja kasutada alternatiivset ravi (vt KLIINILINE FARMAKOLOOGIA, eripopulatsioonid, suitsetamine). Exubera ohutus ja efektiivsus suitsetavate patsientide osas pole tõestatud.
Exubera on suurte erinevuste tõttu vastunäidustatud ebastabiilse või halvasti kontrolli all oleva kopsuhaigusega patsientidel kopsufunktsioonis, mis võib mõjutada Exubera imendumist ja suurendada hüpoglükeemia või hüperglükeemia.
ülaosa
Hoiatused
Exubera erineb tavalisest humaaninsuliinist selle kiire toime alguses. Söömisinsuliinina kasutamisel tuleb Exubera annus anda 10 minuti jooksul enne sööki.
Hüpoglükeemia on insuliinravi, sealhulgas Exubera, kõige sagedamini teatatud kõrvaltoime. Hüpoglükeemia ajastus võib erinevates insuliinipreparaatides erineda.
I tüüpi diabeediga patsiendid vajavad piisava glükoosikontrolli säilitamiseks ka pikema toimeajaga insuliini.
Igasugust insuliini vahetamist tuleb teha ettevaatlikult ja ainult arsti järelevalve all. Insuliini tugevuse, tootja, tüübi (nt tavaline, NPH, analoogid) või liigi (loomne, inimene) muutused võivad põhjustada vajaduse annuse muutmiseks. Võib osutuda vajalikuks kohandada samaaegset suukaudset diabeedivastast ravi.
Kõigil diabeediga patsientidel on soovitatav jälgida glükoosi.
Kuna Exubera mõjutab kopsufunktsiooni, tuleb enne Exubera-ravi alustamist kõigil patsientidel kontrollida kopsufunktsiooni (vt ETTEVAATUSABINÕUD: Kopsufunktsioon).
Exubera kasutamist patsientidel, kellel on põhihaigused, näiteks astma või KOK, ei soovitata, kuna Exubera ohutus ja efektiivsus selles populatsioonis pole tõestatud (vt ETTEVAATUSABINÕUD: Kopsuhaigus).
Exubera kliinilistes uuringutes on Exuberaga ravitud patsientidel esinenud 6 värskelt diagnoositud kopsu esmase pahaloomulisuse juhtu ja 1 võrdlevalt diagnoositud patsiendi seas hiljuti diagnoositud haigusjuht. Samuti on turustamisjärgselt teatatud kopsu primaarse pahaloomulisuse esinemisest Exubera-ravi saanud patsiendil. Exubera kontrollitud kliinilistes uuringutes oli uue primaarse kopsuvähi esinemissagedus uuritava ravimi 100 patsiendiaasta kohta 0,13 (5 juhtu üle 3900 patsiendiaasta) Exubera-ravi saanud patsientide puhul ja 0,02 (1 juhtum üle 4100 patsiendiaasta) võrdlusravi saanud patsientide puhul. Juhtumeid oli liiga vähe, et teha kindlaks, kas nende sündmuste ilmnemine on seotud Exuberaga. Kõigil patsientidel, kellel diagnoositi kopsuvähk, oli varasemalt olnud suitsetamine.
ülaosa
Ettevaatusabinõud
Üldine
Nagu kõigi insuliinipreparaatide puhul, võib ka Exubera toime aeg erinevatel inimestel või ühe ja sama inimese eri aegadel varieeruda. Insuliini annuse kohandamine võib olla vajalik, kui patsiendid muudavad oma füüsilist aktiivsust või tavalist söögikava. Insuliinivajadus võib muutuda selliste perioodiliste seisundite korral nagu haigus, emotsionaalsed häired või stress.
Hüpoglükeemia
Nagu kõigi insuliinipreparaatide puhul, võivad Exubera manustamisega kaasneda hüpoglükeemilised reaktsioonid. Seerumi glükoosikontsentratsiooni kiired muutused võivad diabeediga inimestel põhjustada hüpoglükeemiaga sarnaseid sümptomeid, sõltumata glükoosisisaldusest. Hüpoglükeemia varajased hoiatavad sümptomid võivad olla teatud tingimustel, näiteks pikad, erinevad või vähem väljendunud diabeedi kestus, diabeetiline närvihaigus, selliste ravimite kasutamine nagu beetablokaatorid või intensiivistunud diabeedikontroll (vt ETTEVAATUSABINÕUD: Ravimite koostoimed). Sellised olukorrad võivad põhjustada tõsise hüpoglükeemia (ja võib-olla teadvuse kaotuse) enne patsientide teadlikkust hüpoglükeemiast.
Neerukahjustus
Neerukahjustusega patsientidega ei ole uuringuid läbi viidud. Nagu teistegi insuliinipreparaatide puhul, võib neerukahjustusega patsientide puhul Exubera annustamisvajadus olla väiksem (vt lõik 4.2) KLIINILINE FARMAKOLOOGIA, Eripopulatsioonid).
Maksakahjustus
Maksakahjustusega patsientidega ei ole uuringuid läbi viidud. Nagu teistegi insuliinipreparaatide puhul, võib maksapuudulikkusega patsientidel Exubera annustamisvajadus olla väiksem (vt lõik 4.2) KLIINILINE FARMAKOLOOGIA, Eripopulatsioonid).
Allergia
Süsteemne allergia
Kliinilistes uuringutes oli Exuberaga ravitud patsientide allergiliste reaktsioonide üldine esinemissagedus sarnane patsientidele, kes kasutasid subkutaanset režiimi tavalise humaaninsuliiniga.
Nagu teistegi insuliinipreparaatide puhul, võib tekkida haruldane, kuid potentsiaalselt tõsine üldine allergia insuliini suhtes, mis võib põhjustada lööve (sh kihelus) kogu kehas, õhupuudus, vilistav hingamine, vererõhu langus, kiire pulss või higistamine. Üldise allergia rasked juhud, sealhulgas anafülaktilised reaktsioonid, võivad olla eluohtlikud. Kui sellised reaktsioonid ilmnevad Exuberast, tuleb Exubera kasutamine lõpetada ja kaaluda alternatiivsete ravimeetodite kasutamist.
Antikehade tootmine
Insuliini antikehad võivad tekkida ravi ajal kõigi insuliinipreparaatidega, sealhulgas Exuberaga. Exubera kliinilistes uuringutes, kus võrdlusaluseks oli subkutaanne insuliin, suureneb insuliini antikehade sisaldus (mida näitavad ka insuliini siduv aktiivsus) oli Exuberat saanud patsientide puhul oluliselt suurem kui subkutaanse insuliini saanud patsientide puhul ainult. Exubera kliiniliste uuringute ajal nende antikehade kliinilisi tagajärgi ei tuvastatud; antikehade moodustumise suurenemise pikaajaline kliiniline tähtsus pole aga teada.
Hingamisteede
Kopsufunktsioon
Kuni kaheaastastes kliinilistes uuringutes näitasid Exuberaga ravitud patsiendid kopsufunktsiooni suuremat langust, täpsemalt sundhingamise maht ühes sekundis (FEV1) ja vingugaasi difusioonivõime (DLCO), kui võrdlusravimiga töödeldud patsiendid. Ravigrupi keskmine erinevus kopsufunktsiooni osas, mis eelistas võrdlusrühma, oli vahemikus esimesed mitu nädalat Exubera-ravi ja see ei muutunud kaheaastase raviperioodi jooksul (Vt KÕRVALTOIMED: Kopsufunktsioon).
Kontrollitud kliiniliste uuringute ajal esines mõlemal ravirühmal üksikpatsientidel märkimisväärset kopsufunktsiooni langust. FEV1 langus võrreldes algtasemega - 20% - viimasel vaatlusel esines 1,5% Exubera-ravi saanud patsientidel ja 1,3% -ga võrdlusravi saanud patsientidest. Langus võrreldes DL algväärtusegaCO - 20% -l viimasel vaatlusel esines 5,1% Exubera-ravi saanud ja 3,6% -l võrdlusravi saanud patsientidest.
Kuna Exubera mõjutab kopsufunktsiooni, tuleb kõigil patsientidel enne Exubera-ravi alustamist hinnata spiromeetriat (FEV1). DL-i hindamineCO tuleks kaaluda. Exubera efektiivsus ja ohutus FEV algväärtusega patsientidel1 või DLCO Ennustatud <70% ei ole kindlaks tehtud ja Exubera kasutamist selles populatsioonis ei soovitata.
Kopsufunktsiooni (nt spiromeetria) hindamine on soovitatav pärast ravi esimest 6 kuud ja pärast seda igal aastal, isegi kopsusümptomite puudumisel. Patsientidel, kellel FEV1 langus algtasemest on umbes 20%, tuleks korrata kopsufunktsiooni teste. Kui kinnitatakse FEV1 languse langus 20% võrreldes algtasemega, tuleb Exubera kasutamine katkestada. Kopsuhaigussümptomite esinemine ja kopsufunktsiooni väiksem langus võivad vajada kopsufunktsiooni sagedasemat jälgimist ja Exubera katkestamise kaalumist.
Aluseline kopsuhaigus
Exubera kasutamist kopsuhaigusega, näiteks astma või KOK-iga patsientidel ei soovitata, kuna Exubera efektiivsus ja ohutus selles populatsioonis pole tõestatud.
Bronhospasm
Exuberat kasutanud patsientidel on harva esinenud bronhospasmi. Sellise reaktsiooniga patsiendid peaksid Exubera kasutamise katkestama ja pöörduma viivitamatult arsti poole. Exubera uuesti manustamine nõuab hoolikat riskihindamist ja seda tuleks teha ainult hoolika meditsiinilise jälgimise all koos sobivate kliiniliste võimalustega.
Kaasaegne hingamisteede haigus
Exuberat on kliiniliste uuringute ajal manustatud patsientidele, kellel on vahelduvad hingamisteede haigused (nt bronhiit, ülemiste hingamisteede infektsioonid, nohu). Neid haigusi põdevatel patsientidel katkestasid 3-4% ajutiselt Exubera-ravi. Exubera-ravi saanud patsientidel ei täheldatud hüpoglükeemia ega halvenenud glükeemilise kontrolli riski suurenemist võrreldes subkutaanse insuliiniga ravitud patsientidega. Kaasuvate hingamisteede haiguste ajal võib olla vajalik vere glükoosikontsentratsiooni tähelepanelik jälgimine ja annuse kohandamine.
Teave patsientidele
Patsiente tuleb juhendada enesejuhtimisprotseduuride, sealhulgas glükoosisisalduse jälgimise osas; õige Exubera sissehingamise tehnika; ning hüpoglükeemia ja hüperglükeemia ravi. Patsiente tuleb juhendada eriolukordade, näiteks vahelduvate haigusseisundite (haigus, stress või emotsionaalsed seisundid) käsitlemisel häired), ebapiisav või vahelejäänud insuliiniannus, suurenenud insuliiniannuse tahtmatu manustamine, ebapiisav toidutarbimine või vahele jäänud söögid.
Patsiente tuleb informeerida, et kliinilistes uuringutes seostati Exubera-ravi kopsufunktsiooni väikese, mitte progresseeruva langusega võrreldes võrdlusraviga. Kuna Exubera mõjutab kopsufunktsiooni, soovitatakse enne Exubera-ravi alustamist teha kopsufunktsiooni testid. Pärast ravi alustamist on soovitatav perioodilised kopsufunktsiooni testid (vt lõik 4.2) ETTEVAATUSABINÕUD Hingamisteede, kopsufunktsioon).
Patsiendid peavad oma arsti teavitama, kui neil on varem olnud kopsuhaigus, kuna Exubera kasutamist ei soovitata kaasuva kopsuhaigusega (nt astma või KOK) patsientidel ning halvasti kontrollitava kopsuhaigusega patsientidel on see vastunäidustatud haigus.
Diabeediga naistel tuleb soovitada oma raviarsti või raseduse planeerimise ajal arsti teavitada.
ülaosa
Ravimite koostoimed
Paljud ained mõjutavad glükoosi metabolismi ja võivad vajada insuliini annuse kohandamist ja eriti hoolikat jälgimist.
Järgnevalt on toodud näited ainete kohta, mis võivad vähendada insuliini veresuhkru taset alandavat toimet, mis võib põhjustada hüperglükeemiat: kortikosteroidid, danasool, diasoksiid, diureetikumid, sümpatomimeetilised ained (nt epinefriin, albuterool, terbutaliin), glükagoon, isoniasiid, fenotiasiini derivaadid, somatropiin, kilpnäärmehormoonid, östrogeenid, progestogeenid (nt suukaudsetes rasestumisvastastes vahendites), proteaasi inhibiitorid ja ebatüüpilised antipsühhootilised ravimid (nt olansapiin ja klosapiin).
Järgnevad näited ainete kohta, mis võivad suurendada insuliini vere glükoosisisaldust langetavat toimet ja vastuvõtlikkust hüpoglükeemiale: suukaudne diabeedivastased tooted, AKE inhibiitorid, disopüramiid, fibraadid, fluoksetiin, MAO inhibiitorid, pentoksüfülliin, propoksüfeen, salitsülaadid ja sulfoonamiid antibiootikumid.
Beeta-blokaatorid, klonidiin, liitiumsoolad ja alkohol võivad insuliini vere glükoosisisaldust vähendavat toimet suurendada või vähendada. Pentamidiin võib põhjustada hüpoglükeemiat, millele võib mõnikord järgneda hüperglükeemia.
Lisaks võivad sümpatolüütiliste ravimite, näiteks beetablokaatorite, klonidiini, guanetidiini ja reserpiini mõjul hüpoglükeemia nähud ja sümptomid väheneda või puududa.
Bronhodilataatorid ja muud inhaleeritavad tooted võivad muuta inhaleeritava humaaninsuliini imendumist (vt lõik 4.2) KLIINILINE FARMAKOLOOGIA, Eripopulatsioonid). Bronhodilataatorite annustamise järjepidev ajastamine võrreldes Exubera manustamisega on soovitatav hoolikalt jälgida veresuhkru kontsentratsiooni ja vajaduse korral annust tiitrida.
Kantserogenees, mutagenees, viljakuse langus
Kaheaastaseid kantserogeensuse uuringuid loomadel ei ole läbi viidud. Insuliin ei olnud Amesi bakteriaalse pöördmutatsiooni katses mutageenne metaboolse aktiveerimise juuresolekul ja puudumisel.
Sprague-Dawley rottidel viidi läbi 6-kuuline korduvannuse toksilisuse uuring insuliini inhalatsioonipulbriga annustes kuni 5,8 mg / kg päevas (võrreldes kliinilise algannus 0,15 mg / kg päevas, oli roti kõrge annus 39 korda või 8,3 korda suurem kliinilisest annusest, mis põhineb kas mg / kg või mg / m2 kehapinna kohta). Cynomolgus ahvidel viidi läbi 6-kuuline korduvannuse toksilisuse uuring inhaleeritava insuliiniga annustes kuni 0,64 mg / kg päevas. Võrreldes kliinilise algannusega 0,15 mg / kg päevas, oli ahvide kõrge annus 4,3 või 1,4 korda suurem kliinilisest annusest, tuginedes kas mg / kg või mg / m2 kehapinna kohta. Need olid hüpoglükeemial põhinevad maksimaalsed talutavad annused.
Võrreldes kontrollloomadega, ei esinenud kummagi liigi raviga seotud kahjulikku toimet kopsufunktsioonile, hingamisteede ega bronhide lümfisõlmede üldisele või mikroskoopilisele morfoloogiale. Samuti ei mõjutanud kummagi liigi kopsu alveolaarses ega bronhiolaarses piirkonnas rakkude proliferatsiooni indekseid.
Kuna rekombinantne humaaninsuliin on identne endogeense hormooniga, ei viidud loomadel läbi reproduktiiv- / viljakuse uuringuid.
Rasedus
Teratogeenne toime
C-kategooria rasedus
Exuberaga ei ole loomade paljunemisuuringuid läbi viidud. Samuti pole teada, kas Exubera võib rasedale manustamisel põhjustada lootekahjustusi või kas Exubera võib mõjutada paljunemisvõimet. Exuberat tohib rasedale anda ainult juhul, kui see on selgelt vajalik.
Imetavad emad
Paljud ravimid, sealhulgas humaaninsuliin, erituvad rinnapiima. Sel põhjusel tuleb Exubera manustamisel imetavale naisele olla ettevaatlik. Imetavad diabeediga patsiendid võivad vajada Exubera annuse, söögiplaani või mõlema kohandamist.
Kasutamine lastel
Exubera pikaajalist ohutust ja efektiivsust lastel ei ole tõestatud (vt KLIINILINE FARMAKOLOOGIA, Eripopulatsioonid).
Geriaatriline kasutamine
Kontrollitud faasi 2/3 kliinilistes uuringutes (n = 1975) manustati Exuberat 266-le 65-aastasele patsiendile ja 30-le 75-aastasele patsiendile. Enamikul neist patsientidest oli II tüüpi diabeet. HbA muutus1C ja hüpoglükeemia määr vanuse järgi ei erinenud.
ülaosa
Kõrvaltoimed
Exubera ohutus üksi või koos nahaaluse insuliini või suukaudsete ravimitega on olnud Hinnati umbes 2500 I või II tüüpi diabeediga täiskasvanud patsiendil, kes olid kokku puutunud Exubera. Ligikaudu 2000 patsienti said Exuberat pikema kui 6 kuu jooksul ja enam kui 800 patsienti rohkem kui 2 aastat.
Mittehingamiselundite kahjulikud sündmused
Muude kui hingamisteede kõrvalnähtude hulgas, mida on kontrollitud 2./3. Faasi kliinilistes uuringutes 1% -l 1977. aastal Exubera-ga ravitud patsientidest, sõltumata põhjuslikkusest, on (kuid pole nendega piiratud) järgmised:
Ainevahetus ja toitumine: hüpoglükeemia (vt HOIATUSED ja ETTEVAATUSABINÕUD)
Keha tervikuna: valu rinnus
Seedetrakt: suukuivus
Spetsiaalsed meeleelundid: keskkõrvapõletik (1. tüüpi laste diabeetikud)
Hüpoglükeemia
Hüpoglükeemia esinemissagedus ja esinemissagedus olid Exubera ja nahaaluse regulaarse humaaninsuliini vahel võrreldavad 1. ja 2. tüüpi diabeediga patsientidel. II tüübi patsientidel, kellel ei suudetud piisava kontrolli all hoida ühekordse suukaudse ravimiga, lisada Exuberat seostati kõrgema hüpoglükeemia määraga kui teise suukaudse lisamise korral agent.
Valu rinnus
Kõrvaltoimetena teatati hulgast erinevatest rindkere sümptomitest ja need rühmitati mittespetsiifilise termini rindkerevalu alla. Neid juhtumeid esines 4,7% Exubera-ravi saanud patsientidest ja 3,2% -l võrdlusrühma patsientidest. Enamik (> 90%) neist juhtudest olid kerged või mõõdukad. Kaks Exubera patsienti ja üks võrdlusrühmas katkestasid valu rinnavalu tõttu. Koronaararterite haigusega seotud kõigi põhjuslike kõrvaltoimete, näiteks stenokardia või müokardiinfarkti esinemissagedus oli Exuberas võrreldav (stenokardia 0,7%; 0,7% müokardiinfarkt) ja võrdlusravim (1,3% stenokardia; 0,7% müokardiinfarkti) ravirühmad.
Kuiv suu
Suukuivus esines 2,4% -l Exubera-ravi saanud patsientidest ja 0,8% -l võrdlusrühma patsientidest. Peaaegu kogu (> 98%) teatatud suukuivus oli kerge või mõõdukas. Ükski patsient ei katkestanud ravi suukuivuse tõttu.
Kõrvasündmused lastel diabeetikutel
Exubera rühmade 1. tüüpi lastel diabeetikutel esines kõrvaga seotud kõrvaltoimeid sagedamini kui ainult 1. tüüpi laste diabeetikutel ravigruppides, kes said ainult nahaalust insuliini. Need sündmused hõlmasid keskkõrvapõletikku (Exubera 6,5%; SC 3,4%), kõrvavalu (Exubera 3,9%; SC 1,4%) ja kõrvahaigused (Exubera 1,3%; SC 0%).
Hingamisteede kahjulikud sündmused
Tabelis 6 on esitatud hingamisteede kõrvaltoimete esinemissagedus iga ravirühma kohta, millest teatati kontrollitud 2. ja 3. faasi kliinilistes uuringutes - 1% kõigist ravigruppidest, sõltumata põhjuslikkusest.
Tabel 6: Hingamiselundite kahjulikud sündmused, millest on teatatud kontrollitud 2. ja 3. faasi kliinilistes uuringutes osalenud ravigrupist - 1%, sõltumata põhjuslikkusest
| Protsent patsientidest, kes teatasid sündmusest | |||||
|---|---|---|---|---|---|
| Ebasoodne sündmus | 1. tüüpi diabeet | 2. tüüpi diabeet | |||
| Exubera N = 698 |
SC N = 705 |
Exubera N = 1279 |
SC N = 488 |
OAs N = 644 |
|
| SC = subkutaanne insuliini võrdlusaine; OA = suukaudsete ainete võrdlusseadmed | |||||
| Hingamisteede nakatumine | 43.3 | 42.0 | 29.2 | 38.1 | 19.7 |
| Köha suurenenud | 29.5 | 8.8 | 21.9 | 10.2 | 3.7 |
| Farüngiit | 18.2 | 16.6 | 9.5 | 9.6 | 5.9 |
| Nohu | 14.5 | 10.9 | 8.8 | 10.5 | 3.0 |
| Sinusiit | 10.3 | 7.4 | 5.4 | 10.0 | 2.3 |
| Hingamishäire | 7.4 | 4.1 | 6.1 | 10.2 | 1.7 |
| Hingeldus | 4.4 | 0.9 | 3.6 | 2.5 | 1.4 |
| Röga suurenenud | 3.9 | 1.3 | 2.8 | 1.0 | 0.5 |
| Bronhiit | 3.2 | 4.1 | 5.4 | 3.9 | 4.0 |
| Astma | 1.3 | 1.3 | 2.0 | 2.3 | 0.5 |
| Ninaverejooks | 1.3 | 0.4 | 1.2 | 0.4 | 0.8 |
| Larüngiit | 1.1 | 0.4 | 0.5 | 0.4 | 0.3 |
| Kopsupõletik | 0.9 | 1.1 | 0.9 | 1.6 | 0.6 |
| Hääle muutmine | 0.1 | 0.1 | 1.3 | 0.0 | 0.3 |
Köha
Kolmes kliinilises uuringus teatasid köha küsimustiku täitnud patsiendid, et köha kipub ilmnema jooksul sekundites kuni minutites pärast Exubera sissehingamist oli peamiselt kerge raskusega ja harva produktiivne loodus. Selle köha esinemissagedus vähenes Exubera jätkuval kasutamisel. Kontrollitud kliinilistes uuringutes katkestas 1,2% patsientidest Exubera ravi köha tõttu.
Hingeldus
Peaaegu kogu (> 97%) hingeldus esines kergel või mõõdukal kujul. Väike arv Exubera-ravi saanud patsiente (0,4%) katkestas hingelduse tõttu ravi, võrreldes 0,1% -ga võrdlusravi saanud patsientidest.
Muud hingamisteede kahjulikud sündmused - farüngiit, suurenenud röga ja ninaverejooks
Enamik neist juhtudest olid kerged või mõõdukad. Väike arv Exuberaga ravitud patsiente katkestas ravi farüngiidi (0,2%) ja röga suurenemise (0,1%) tõttu; ükski patsient ei katkestanud ravi ninaverejooksu tõttu.
Kopsufunktsioon
Exubera toimet hingamiselunditele hinnati enam kui 3800 patsiendil kontrollitud 2. ja 3. faasi kliinilistes uuringutes (milles Exuberaga raviti 1977 patsienti). Kuni kaheaastased randomiseeritud avatud kliinilistes uuringutes Exuberaga ravitud patsiendid demonstreeris kopsufunktsiooni suuremat langust, eriti sunnitud väljahingatava ruumala ühes teine (FEV1) ja vingugaasi difusioonivõime (DLCO) kui võrdlusravi saanud patsientidel. Ravi rühmade keskmised erinevused FEV-s1 ja DLCO, täheldati Exubera-ravi esimesel paaril nädalal ja need ei edenenud kaheaastase raviperioodi jooksul. Ühes lõppenud kontrollitud kliinilises uuringus II tüüpi diabeediga patsientidega pärast kaheaastast Exubera-ravi näitasid patsiendid FEV-i ravirühmade erinevuse kadumist1 kuus nädalat pärast ravi katkestamist. Exubera mõju kopsutalitlusele 1. tüüpi diabeediga patsientidel ei ole pärast pikaajalist ravi uuritud.
Joonised 3 kuni 6 näitavad keskmist FEV-d1 ja DLCO muutus võrreldes algtasemega võrreldes kahe käimasoleva randomiseeritud, avatud, kaheaastase uuringuga 580 I tüüpi patsiendil ja 620 II tüüpi diabeediga patsiendil.
Joonis 3: Muutus algtaseme FEV1 (L) tasemelt 1. tüüpi diabeediga patsientidel (keskmine +/- standardhälve)
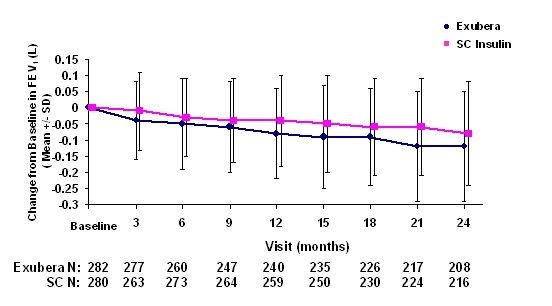
Joonis 4: Muutus II tüübi diabeediga patsientide FEV1 (L) algväärtusest (keskmine +/- standardhälve)
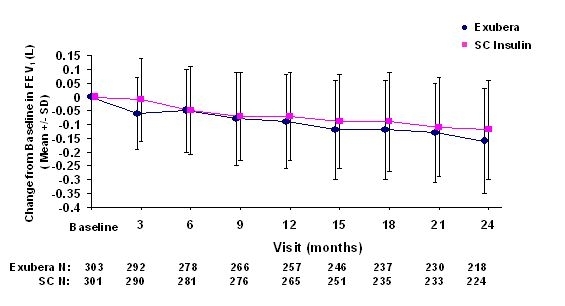
Pärast 2-aastast Exubera-ravi 1. ja 2. tüüpi diabeediga patsientidel oli erinevus ravirühmade vahel oli keskmine muutus võrreldes algtasemega FEV1 umbes 40 ml, eelistades komparaator.
Joonis 5: Muutus algtaseme DLco väärtusest (ml / min / mmHg) 1. tüüpi diabeediga patsientidel (keskmine +/- standardhälve)
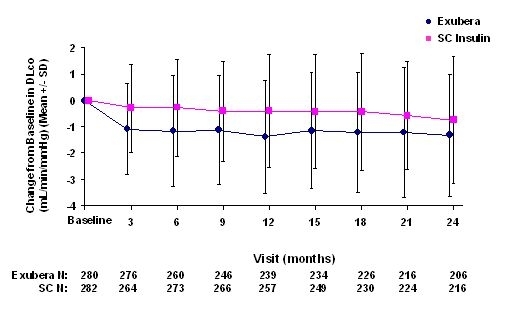
Joonis 6: Muutus algtaseme DLco väärtusest (ml / min / mmHg) II tüüpi diabeediga patsientidel (keskmine +/- standardhälve)
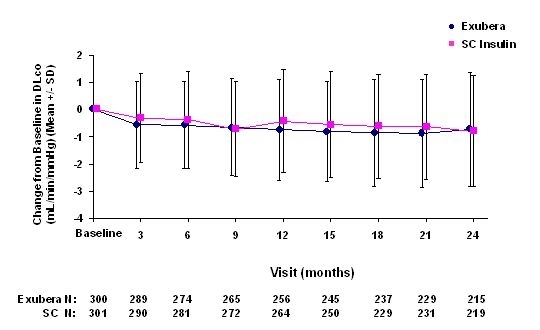
Pärast 2-aastast Exubera-ravi oli erinevus ravigruppide vahel keskmise muutuse osas võrreldes algväärtusega DLCO oli umbes 0,5 ml / min / mmHg (1. tüüpi diabeet), eelistades võrdlusravimit, ja umbes 0,1 ml / min / mmHg (2. tüüpi diabeet), eelistades Exuberat.
Kaheaastase kliinilise uuringu ajal esines mõlemas ravirühmas üksikpatsientidel märkimisväärset kopsufunktsiooni langust. Langus võrreldes algväärtusega FEV1 - 20% -l viimasest vaatlusest esines 1,5% Exubera-ravi saanud patsientidest ja 1,3% -ga võrdlusravi saanud patsientidest. Langus võrreldes DL algväärtusegaCO - 20% -l viimasel vaatlusel esines 5,1% Exubera-ravi saanud ja 3,6% -l võrdlusravi saanud patsientidest.
ülaosa
Üleannustamine
Hüpoglükeemia võib tekkida insuliini ülemäärase koguse tõttu, võrreldes toidu tarbimise, energiakulu või mõlemaga.
Hüpoglükeemia kergeid kuni mõõdukaid episoode saab tavaliselt ravida suu kaudu manustatava glükoosiga. Vajalikuks võib osutuda ravimite annuse, söögikordade või treeningu kohandamine.
Raskeid hüpoglükeemia episoode koos kooma, krampide või neuroloogiliste häiretega võib ravida intramuskulaarse / nahaaluse glükagooni või kontsentreeritud intravenoosse glükoosiga. Vajalik võib olla pidev süsivesikute tarbimine ja jälgimine, kuna hüpoglükeemia võib ilmse kliinilise taastumise korral korduda.
ülaosa
Annustamine ja manustamine
Exuberal, nagu kiiretoimelistel insuliinianaloogidel, on glükoosisisaldust langetav toime kiirem kui subkutaanselt süstitud regulaarsel iniminsuliinil. Exubera glükoosisisaldust vähendav toime on võrreldav subkutaanselt süstitava tavalise iniminsuliiniga ja pikem kui kiiretoimelise insuliiniga. Exubera annused tuleb manustada vahetult enne sööki (mitte rohkem kui 10 minutit enne iga sööki).
I tüüpi diabeediga patsientidel tuleb Exuberat kasutada režiimides, mis sisaldavad pikema toimeajaga insuliini. II tüüpi diabeediga patsientide puhul võib Exuberat kasutada monoteraapiana või kombinatsioonis suukaudsete ravimite või pikema toimeajaga insuliiniga.
Kuna Exubera mõjutab kopsufunktsiooni, tuleb enne Exubera-ravi alustamist kõigil patsientidel kontrollida kopsufunktsiooni. Exubera'ga ravitavatel patsientidel on soovitatav perioodiliselt jälgida kopsufunktsiooni (vt ETTEVAATUSABINÕUD, Kopsufunktsioon).
Exubera on ette nähtud inhalatsiooni teel manustamiseks ja seda võib manustada ainult Exubera abil® Sissehingaja. Vt Exubera ravijuhend Exubera kirjeldus® Inhalaator ja juhised inhalaatori kasutamise kohta.
Algse söögieelse eksubera annuse arvutamine
Exubera algannus tuleb individuaalselt määrata ja määrata vastavalt arsti soovitustele vastavalt patsiendi vajadustele. Soovitatavad söögieelsed algannused põhinevad kliinilistel uuringutel, kus patsientidel paluti süüa kolm söögikorda päevas. Algse söögieelse annuse võib arvutada järgmise valemi abil: [kehakaal (kg) X 0,05 mg / kg = söögieelne annus (mg)], ümardatud lähima täisarvuni (nt 3,7 mg, ümardatud allapoole 3-ni) mg).
Ligikaudsed juhised söögieelsete Exubera algannuste jaoks, lähtudes patsiendi kehakaalust, on toodud tabelis 7:
Tabel 7: Ligikaudne juhend esialgseks söögieelseks eksubera annuseks (põhineb patsiendi kehakaalul)
| Patsiendi kaal (kg) |
Patsiendi kaal (nael) |
Algannus toidukorra kohta | 1 mg villide arv annuse kohta | 3 mg villide arv annuse kohta |
|---|---|---|---|---|
| 30 kuni 39,9 kg | 66 - 87 naela | 1 mg söögikorra kohta | 1 | - |
| 40 kuni 59,9 kg | 88 - 132 naela | 2 mg söögikorra kohta | 2 | - |
| 60 kuni 79,9 kg | 133 - 176 naela | 3 mg söögikorra kohta | - | 1 |
| 80 kuni 99,9 kg | 177 - 220 naela | 4 mg söögikorra kohta | 1 | 1 |
| 100 kuni 119,9 kg | 221–264 naela | 5 mg söögikorra kohta | 2 | 1 |
| 120 kuni 139,9 kg | 265–308 naela | 6 mg söögikorra kohta | - | 2 |
1 mg Exubera inhaleeritava insuliini blister on umbes ekvivalentne 3 RÜ subkutaanselt süstitava tavalise iniminsuliiniga. 3 mg Exubera inhaleeritava insuliini blister on umbes ekvivalentne 8 RÜ-ga subkutaanselt süstitud tavalise humaaninsuliiniga. Tabelis 8 on toodud tavalise subkutaanse humaaninsuliini ligikaudne RÜ annus Exubera inhaleeritavate insuliiniannuste 1 mg kuni 6 mg jaoks.
Tabel 8: Inimese tavalise subkutaanse insuliini ligikaudne ekvivalentne RÜ annus Exubera inhaleeritavate insuliiniannuste korral vahemikus 1 mg kuni 6 mg
| Annus (mg) | Ligikaudne regulaarne insuliini SC annus RÜ-s | 1 mg Exubera blistrite arv annuse kohta | 3 mg Exubera blistrite arv annuse kohta |
|---|---|---|---|
| 1 mg | 3 | 1 | - |
| 2 mg | 6 | 2 | - |
| 3 mg | 8 | - | 1 |
| 4 mg | 11 | 1 | 1 |
| 5 mg | 14 | 2 | 1 |
| 6 mg | 16 | - | 2 |
Patsiendid peaksid ühendama 1 mg ja 3 mg blistrid nii, et ühe annuse kohta võetaks võimalikult vähe villid (nt 4 mg annus tuleb manustada ühe 1 mg blistrina ja ühe 3 mg blistrina). Kolme 1 mg ühikannusega blistri järjestikuse sissehingamise tulemuseks on oluliselt suurem insuliini ekspositsioon kui ühe 3 mg ühikannusega blistri sissehingamine. Seetõttu ei tohiks kolme 1 mg annust asendada ühe 3 mg annusega (vt punkt 4.2) KLIINILINE FARMAKOLOOGIA, Farmakokineetika). Kui patsient on stabiliseerunud annustamisskeemi järgi, mis sisaldab 3 mg blistrit ja 3 mg blistrit muutudes ajutiselt kättesaamatuks, võib patsient ajutiselt asendada kaks 1 mg blistrit ühega 3 mg vill. Vere glükoosisisaldust tuleb hoolikalt jälgida.
Nagu kõigi insuliinide puhul, hõlmavad täiendavad tegurid, mida tuleks Exubera algannuse määramisel arvestada, kuid ei piirdu patsiendi praeguse glükeemilise kontrolliga, varasema ravivastusega insuliinile, diabeedi kestusega ning dieedi ja treenimisega harjumused.
Annuse tiitrimise kaalutlused
Pärast Exubera-ravi alustamist võib osutuda vajalikuks annuse kohandamine, nagu ka teiste glükoosisisaldust langetavate ravimite korral patsiendi vajadus (nt vere glükoosikontsentratsioonid, söögi suurus ja toitainete koostis, kellaaeg ja hiljutine või eeldatav) harjutus). Iga patsiendi tiitrimine peab olema optimaalne annus, mis põhineb veresuhkru jälgimise tulemustel.
Nagu kõigi insuliinide puhul, võib ka Exubera toime aeg erinevatel inimestel või ühe ja sama inimese eri aegadel varieeruda.
Exuberat võib kasutada korduvate hingamisteede haiguste (nt bronhiit, ülemiste hingamisteede infektsioon, riniit) ajal. Vajalik võib olla individuaalne veresuhkru kontsentratsiooni tähelepanelik jälgimine ja annuse kohandamine. Inhaleeritavaid ravimeid (nt bronhodilataatoreid) tuleb manustada enne Exubera manustamist.
ülaosa
Kuidas komplektis
Exubera (inimese insuliin [rDNA päritolu). Inhalatsioonipulber on saadaval 1 mg ja 3 mg ühikannusega blistrites. Blistrid jaotatakse perforeeritud kaartidele, mis sisaldavad kuut ühikannusega blistrit (PVC / alumiinium). Neid kahte tugevust eristavad värvitrükk ja kombatavad märgid, mida saab eristada puudutusega. 1 mg blistrid ja vastavad perforeeritud kaardid on trükitud rohelise tindiga ja kaardid on tähistatud ühe tõstetud ribaga. 3 mg blistrid ja vastavad perforeeritud kaardid on trükitud sinise tindiga ja kaardid on tähistatud kolme tõstetud ribaga.
Viis blisterkaarti on pakendatud läbipaistvast plastikust (PET) termoformistatud alusesse. Iga PET-kandik sisaldab ka kuivatusainet ja see on kaetud läbipaistvast plastikust (PET) kaanega. Viiest blisterkaardist koosnev salv (30 ühikannusega blistrit) suletakse kuivatusainega fooliumlaminaadikotti.
Exubera (iniminsuliin [rDNA päritolu)) sissehingatava pulbri villid, Exubera® Inhalaator ja Exubera asendaja® Exubera-ravi alustamiseks on vajalikud vabastamisüksused ja need on toodud Exubera komplektis. Täielikult kokkupandud Exubera® Inhalaator koosneb inhalaatori alusest, kambrist ja Exuberast® Vabastusüksus. Täielikult kokku pandud inhalaator on pakendatud asenduskambriga ja on saadaval Exubera komplektis ning eraldi seadmena. Koda on saadaval ka eraldi komponendina.
Exubera® Vabastusüksused pakitakse eraldi suletud termoformitud alusesse. Üks Exubera® Vabastusseade on lisatud täielikult komplekteeritud inhalaatorisse. Exubera komplektis ja igas kombinatsioonikomplektis on kaks täiendavat vabastamisüksust. Exubera väljalaskeüksused on saadaval ka eraldi.
Nende konfiguratsioonide kirjeldust leiate tabelitest 9 ja 10.
Tabel 9
| Exubera (iniminsuliin [rDNA päritolu]) inhalatsioonipulber on saadaval järgmiselt: | ||
|---|---|---|
| Kirjeldus | Sisu | NDC |
| Exubera KIT | 1 Exubera inhalaator 1 Asenduskoda 1 mg - 180 blistrit 3 mg - 90 blistrit 2 Exubera® Vabastage ühikud |
0069-0050-85 |
| Exubera kombinatsioonipakett 12 | 1 mg - 90 blistrit 3 mg - 90 blistrit 2 Exubera® Vabastage ühikud |
0069-0050-19 |
| Exubera kombinatsioonipakett 15 | 1 mg - 180 blistrit 3 mg - 90 blistrit 2 Exubera® Vabastage ühikud |
0069-0050-53 |
| Exubera 1 mg patsiendi pakend | 90 - 1 mg 2 Exubera® Vabastage ühikud |
0069-0707-37 |
| Exubera 3 mg patsiendi pakend | 90 - 3 mg 2 Exubera® Vabastage ühikud |
0069-0724-37 |
Tabel 10
| Exubera® Inhalaator ja komponendid on saadaval järgmiselt: | ||
|---|---|---|
| Kirjeldus | Sisu | NDC |
| Exubera® Sissehingaja ja koda | 1 Exubera® Sissehingaja 1 Asenduskoda |
0069-0054-19 |
| Exubera® Vabastage ühikud | 2 Exubera® Vabastage ühikud | 0069-0097-41 |
| Exubera® Koda | 1 Asenduskoda | 0069-0061-19 |
Blisterpakend
Mittekasutatud (avamata): hoida kontrollitud toatemperatuuril 25 ° C (77 ° F); ekskursioonid on lubatud temperatuurini 15-30 ° C (59-86 ° F) [vt USP kontrollitud ruumi temperatuuri]. Mitte külmuda. Mitte hoida külmkapis.
Kasutamine: kui fooliumist ümbris on avatud, tuleb ühikannusega blistrit kaitsta niiskuse eest, hoida temperatuuril 25 ° C (77 ° F); ekskursioonid on lubatud temperatuurini 15-30 ° C (59-86 ° F) [vt USP kontrollitud ruumi temperatuuri]. Mitte külmuda. Mitte hoida külmkapis. Ühikdoosilised blistrid tuleb ära kasutada 3 kuu jooksul pärast fooliumkatte avamist. Niiskuse eest kaitsmiseks viige villid korki tagasi. Täiendava ettevaatusega tuleks vältida niiske keskkonna, nt. aurupealne duširuum.
Visake blister ära, kui see on külmunud.
Inhalaatorite hoidmine
Hoida kontrollitud toatemperatuuril 25 ° C (77 ° F); ekskursioonid on lubatud temperatuurini 15-30 ° C (59-86 ° F) [vt USP kontrollitud ruumi temperatuuri]. Mitte külmuda. Mitte hoida külmkapis.
Exubera® Inhalaatorit saab kasutada kuni ühe aasta jooksul pärast esmakordset kasutamist.
Exubera asendamine® Vabastusüksus
Exubera® Väljalaskeüksus Exuberas® Inhalaatorit tuleb vahetada iga 2 nädala järel.
Hoida lastele kättesaamatus kohas
Ainult Rx

LAB-0331-12.0
viimane redaktsioon 04/2008
Exubera, inimese insuliin [rDNA päritolu] Patsiendi teave (lihtsas inglise keeles)
Üksikasjalik teave diabeedi märkide, sümptomite, põhjuste, ravi kohta
Selles monograafias sisalduv teave ei ole mõeldud hõlmama kõiki võimalikke kasutusviise, juhiseid, ettevaatusabinõusid, ravimite koostoimet või kahjulikke mõjusid. See teave on üldistatud ja ei ole mõeldud spetsiaalse meditsiinilise nõuandena. Kui teil on küsimusi kasutatavate ravimite kohta või soovite lisateavet, pidage nõu arsti, apteekri või meditsiiniõega.
tagasi: Sirvige kõiki diabeediravimeid



